Gebruik van antibiotica in de veehouderij en resistentie, 1999 - 2018
U bekijkt op dit moment een archiefversie van deze indicator. De actuele indicatorversie met recentere gegevens kunt u via deze link bekijken.
Sinds 2007 is het gebruik van antibiotica in de veehouderij flink afgenomen. Na de snelle daling van het gebruik is deze afgevlakt en stagneert sinds 2016. Veelvuldig gebruik van antibiotica leidt tot resistentie van bacteriën. Vanaf 2012-2013 neemt ook de resistentie duidelijk af. Dit is goed nieuws omdat in de veehouderij en de humane gezondheidszorg deels dezelfde antibiotica worden gebruikt, en dus een verlies aan werkzame antibiotica ook een risico voor de mens is.
Daling verkoop antibiotica stagneert sinds 2016
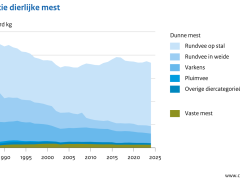
Het EU-verbod om antibiotica als groeibevorderaar aan diervoeders toe te voegen is vanaf 1999 stapsgewijs ingevoerd, met een volledig verbod vanaf 2006. Omdat antibiotica nu vaker gebruikt werden voor de behandeling van zieke dieren bleef het totale gebruik ongeveer gelijk. Daarna is het gebruik van antibiotica in de Nederlandse veehouderij, na een maximum in 2007, steeds verder afgenomen.
Sinds 2009 is de verkoop van antibiotica voor de veehouderij in 2018 met bijna 64% gedaald (MARAN-2019). Na een aanvankelijk snelle daling van het gebruik van antibiotica van 2009 tot 2012 is deze afgevlakt en stagneert sinds 2016. Dit blijkt uit verkoopcijfers van de branchevereniging Veterinaire Farmacie (FIDIN).
Grote verschillen tussen sectoren en bedrijven
Uit de jaarlijkse monitoring van de Stichting Autoriteit Diergeneesmiddelen (SDa) blijkt dat het aantal behandeldagen met antibiotica ten opzichte van 2009 het meest gedaald is bij vleeskuikens, namelijk ongeveer 70%. In de varkenshouderij was deze daling ruim 55% (SDa, 2019). In de vleeskalverhouderij was de daling het minst met 44%. Vleeskalverhouders en kalkoenhouders behandelden hun dieren in 2018 het vaakst, met respectievelijk 19 en 17 behandeldagen per jaar. Melkkoeien kregen met ruim 3 behandeldagen per jaar het minst vaak antibiotica toegediend.
Het gebruik per (kg levend) dier ligt in Nederland beneden het Europees gemiddelde en ver beneden het gebruik van antibiotica in landen als België, Italië en Spanje (EMA, 2018).
Alleen bij melkveehouders is sprake van een stabiel en verantwoord laag gebruik over een reeks van jaren. Voor de overige veesectoren bestaat er een aanzienlijke variatie in het gebruik binnen de sector. Een verdere verlaging van het aandeel bedrijven dat de dieren vaak behandelt met antibiotica (veelgebruikers) is daar wenselijk (EZ, 2016; SDa, 2017). Het percentage veelgebruikers van antibiotica was in 2018 voor de meeste sectoren minder dan 10% van het aantal bedrijven in de sector en ook hier lijkt de daling te stagneren. Omdat de huidige criteria voor veelgebruik niet meer richtinggevend zijn deze aangescherpt (SDa, 2019). Volgens de nieuwe criteria varieerde het percentage veelgebruikers in 2018 van 60%-70% van de bedrijven met jonge kalveren en kalkoenen tot 0%-3% van de bedrijven met respectievelijk melkvee en jongvee. Bij het merendeel van de sectoren ligt het percentage veelgebruikers volgens de nieuwe criteria rond de 30% (SDa, 2019).
Bacteriële resistentie tegen antibiotica in vee neemt af
Veelvuldig of onzorgvuldig gebruik van antibiotica in de veehouderij leidt tot bacteriële resistentie (Mevius, 2008). Na de daling van het gebruik is sinds 2012-2013 ook de resistentie duidelijk afgenomen bij alle diercategorieën (MARAN-2019). Antibioticaresistentie is het hoogst bij dieren die voor de vleesproductie worden gehouden. Een van de bacteriën die deze resistentie heeft ontwikkeld, is de indicator darmbacterie E. coli (zie onderstaande figuur). Het hoogste niveau van resistentie in deze bacterie doet zich voor bij vleeskalveren en vleeskuikens: 22% van de E. coli bacteriën was in 2018 resistent tegen vier of meer groepen van antibiotica. In 2010 was de resistentie bij vleeskuikens nog meer dan 60%.
Het gebruik van antibiotica in de veehouderij is nog steeds hoger dan in de humane gezondheidszorg. Nederland kent met minder dan 11 standaarddoseringen per 1000 inwoners per dag het laagste gebruik binnen Europa bij mensen (NETHMAP, 2019). Ter vergelijking: het aantal standaarddoseringen per 1000 dieren in de intensieve veehouderij in 2018 loopt uiteen van ongeveer 10 voor vleesvarkens en 30 voor vleeskuikens tot 50 standaarddoseringen per 1000 dieren per dag voor vleeskalveren.
Risico's voor de volksgezondheid
Mensen en dieren dragen bacteriën bij zich en van nature komt resistentie bij al deze bacteriën voor. Veel bacteriën zijn onschadelijk maar sommige kunnen ziekten veroorzaken. Het antibioticagebruik in de veehouderij brengt potentieel risico's voor de volksgezondheid met zich mee omdat veelvuldig en onzorgvuldig gebruik ertoe kan leiden dat ziekmakende bacteriën, resistent worden tegen veel gebruikte antibiotica. In de veehouderij en de humane gezondheidszorg worden deels dezelfde antibiotica gebruikt. Een beperktere beschikbaarheid van werkzame antibiotica bemoeilijkt de behandeling van infecties bij mensen.
De risico's zijn hoger voor mensen met een verlaagde weerstand. Sinds 2016 worden de voor de mens belangrijke zogenaamde derde en vierde generatie middelen nauwelijks nog gebruikt voor dieren.
Resistente bacteriën kunnen zich verspreiden van mens op mens, maar ook via dieren, voedsel en het milieu. Het risico van met voedsel overdraagbare besmetting neemt toe naarmate de hygiëne in de keuken meer te wensen overlaat. Voorbeelden zijn Salmonella en Campylobacter.
MRSA-bacterie
De meest bekende resistente bacteriën die zowel bij mensen als dieren voorkomen zijn de MRSA-bacterie en ESBL-producerende bacteriën. De MRSA-bacterie (ook wel ziekenhuisbacterie genoemd) is ongevoelig voor de zogenoemde beta-lactam-antibiotica, die belangrijk zijn voor de behandeling van ernstige infecties. Omdat de besmettelijkheid van de variant van MRSA die bij dieren wordt gevonden, minder is dan van de 'gewone' MRSA komen ernstige infecties bij mensen met verminderde weerstand (zoals in ziekenhuizen) zelden voor (Gezondheidsraad, 2015). Ongeveer 10-15% van het aantal humane MRSA-infecties (vooral huidinfecties) betreft de veegerelateerde variant van MRSA. Dit is duidelijk hoger dan in andere Europese landen (van Cleef et al., 2011). Ruim 60 procent van de veehouders in Nederland is besmet, evenals ongeveer 10 procent van hun gezinsleden (van Cleef, 2016). Buiten deze groep komt de veegerelateerde MRSA veel minder voor.
ESBL-producerende bacteriën
Ook ontstaat er risico voor de volksgezondheid als bij dieren resistentiegenen voorkomen in de darmbacteriën, bijvoorbeeld in E. coli, die overdraagbaar zijn naar de menselijke darmflora. Dit zou kunnen plaatsvinden bij ESBL's (Extended Spectrum Beta-lactamases). ESBL's zijn enzymen in bacteriën die alle beta-lactam-antibiotica kunnen inactiveren. De genen die voor productie van deze enzymen zorgen, zijn meestal overdraagbaar tussen bacteriën. Dat maakt een snelle verspreiding mogelijk, onder meer van dier naar mens. De Gezondheidsraad (2015) beschouwt ESBL-producerende bacteriën als het grootste risico voor de volksgezondheid waar het gaat om antibiotica gerelateerde risico's.
Het voorkomen van humane besmettingen met ESBL-producerende bacteriën (risicogroepen zoals veehouders uitgezonderd) wordt voor meer dan 60 procent veroorzaakt door contact met andere mensen. Bijna een vijfde (19%) van de besmettingen loopt deze groep op via voedsel, acht procent door contact met huisdieren en vier procent door niet-beroepsmatig contact met vee. Toch blijven niet-menselijke bronnen van essentieel belang. Zonder deze bronnen zouden ESBL-bacteriën waarschijnlijk verdwijnen uit de menselijke populatie. Daarom blijft continue monitoring noodzakelijk (Mughini-Gras et al., 2019). Bij veehouders is contact met vee waarschijnlijk de belangrijkste bron (ESBLAT 2018).
Antibioticaresistentie verspreidt zich in het milieu
Ook bij bacteriën in het milieu (bodem, water, lucht) komt van nature resistentie voor. Echter het gebruik van antibiotica voor mensen en dieren veroorzaakt de verspreiding van resten van antibiotica en van resistente bacteriën en resistentiegenen in het milieu. Dit heeft als risico dat er zich in de pool van resten van antibiotica en resistentiegenen in het milieu nieuwe resistenties kunnen ontwikkelen door mutaties en genoverdracht. Het is nog niet bekend of het milieu in vergelijking met de hierboven genoemde risico's vanuit de veehouderij een relevante route van overdracht van resistentie naar de mens vormt (Huijbers et al., 2015) (Lahr et al., 2019).
De overdracht van resistente bacteriën en resistentiegenen via het milieu naar de mens zou plaats kunnen vinden door verspreiding van stof uit stallen en via mest en afvalwater.
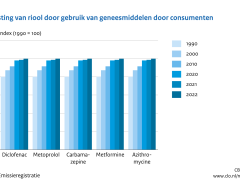
TNO heeft resten van antibiotica aangetroffen in grondwater tot 40 jaar oud (Kivits et al., 2017). De omstandigheden waaronder deze zijn aangetroffen wijzen op dierlijke mest als bron. Behalve in mest worden resten van antibiotica ook aangetroffen in afvalwater en bodem. Ook resistente bacteriën en resistentiegenen worden aangetroffen in afvalwater (in bijna alle monsters zowel ongezuiverd als na zuivering) en dierlijke mest (het meest in vleeskalvermest: 75% van de monsters) (Schmitt et al., 2017). Verdere verspreiding is opgetreden naar oppervlaktewater (Blaak et al., 2010) en bodem. Het voorkomen van antibioticaresten kan van invloed zijn op bodemfuncties van bacteriën en op concentraties van antibiotica in gewassen. Over de ecologische en landbouwkundige consequenties hiervan is nog veel onduidelijk (Singer et al., 2016) (Lahr et al., 2019). Ook uit onderzoek in Nederland is gebleken dat de hoeveelheid resistentiegenen in de bodem in de periode 1940-2008 is toegenomen (Knapp et al., 2010). Het onderzoek naar de ecologische risico's bij de toelating voor antibiotica als diergeneesmiddelen maakt een afweging van baten en risico's. Meestal worden risico-verminderende maatregelen voorgesteld (Lahr et al., 2019).
Gezondere dieren
De gezondheid van dieren is in de loop van de tijd waarschijnlijk verbeterd. Alhoewel exacte meetgegevens ontbreken, zijn er diverse ontwikkelingen die daarop duiden (Leenstra et al., 2010). Ondanks positieve ontwikkelingen leiden dierziekten steeds vaker tot maatschappelijke onrust. Het voorbeeld van de Q-koorts heeft laten zien dat sommige dierziekten een serieuze bedreiging voor de menselijke gezondheid kunnen zijn.
Ook antibiotica dragen bij aan de gezondheid van dieren. Antibiotica zijn effectief, betrouwbaar en goedkoop (PBL, 2010).
Beleid voor antibioticagebruik in de veehouderij
De Nederlandse overheid heeft de verantwoordelijkheid voor het terugdringen van het gebruik van antibiotica bij de veehouderijsector gelegd. De overheid ziet toe op zorgvuldig gebruik. Genomen maatregelen zijn o.a. registratie van het gebruik en van het voorschrijfgedrag, vaste contracten tussen veehouder en veearts, beperking van groepsmedicatie en een verbod op het toedienen van antibiotica door de veehouder zelf als hij geen bedrijfsgezondheid- en behandelplan heeft (EZ, 2014). De nieuwe EU-Verordening Diergeneesmiddelen (EU, 2019) bevat vergelijkbare regels, zoals het verbod op preventief antibioticumgebruik, en deze regels gelden vanaf 2022 - in de hele EU. Mogelijkheden om antibioticagebruik verantwoord terug te dringen zijn onder meer goede voeding, betere hygiëne, goed geventileerde stallen en het vermijden van stress voor de dieren. De verschillende veehouderijsectoren hebben hiervoor in 2016 plannen gemaakt. De SDa heeft in samenwerking met de veehouderijsectoren in 2018 nieuwe richtinggevende benchmarkwaarden opgesteld voor veelgebruik van antibiotica (SDa, 2018). De sectoren hebben op basis hiervan reductiedoelen voor 2024 vastgesteld (SDa, 2019). De afgesproken sectordoelen, die vooral gericht zijn op het terugdringen van het aantal veelgebruikers, vervangen de generieke 70% reductiedoelstelling voor 2020 ten opzichte van 2009 (LNV, 2019). Met bijna 64% reductie in 2018 ten opzichte van 2009 was deze doelstelling (nog) niet bereikt. Volgens de nieuwe sectordoelen zullen de pluimveehouderij, varkenshouderij en kalverhouderij het aantal veelgebruikers verminderen met 50% in 2024 ten opzichte van het aantal in het jaar 2017. De nieuwe benchmarkwaarden voor bedrijven met vleeskalveren, biggen, kalkoenen en konijnen zijn nog steeds hoger dan wenselijk en zullen daarom na 2020 verder naar beneden worden bijgesteld. Daarnaast zal de kalverhouderij het antibioticagebruik reduceren met 15% in de periode 2017- 2022 mits de bestrijding van twee belangrijke kalverziekten succesvol is.
Bronnen
- Blaak H., F.M. Schets, R. Italiaander, H. Schmitt en A.M. de Roda Husman (2010) Antibioticaresistente bacteriën in Nederlands oppervlaktewater in veeteeltrijk gebied. RIVM rapport 703719031
- Baede VO, Wagenaar JA, Broens EM, Duim B, Dohmen W, Nijsse R e.a. Longitudinal study of extended-spectrum-beta-lactamase- and AmpC-producing Enterobacteriaceae in household dogs. Antimicrobial Agents Chemotherapy 2015; 59(6): 3117-3124.
- Bondt, N., L.F. Puister, L. Ge, H.B. van der Veen, R.H.M. Bergevoet, B.E. Douma, A.L.J. van Vliet & K.W. Wehling (2012) Trends in veterinary antibiotic use in the Netherlands 2005-2011
- Cleef, B.A.G.L. van (2016) MRSA in pig farms: human epidemiology.
- Cleef, B.A.G.L. van, et al., (2011). Livestock-associated Methicillin-Resistant Staphylococcus aureus in Humans, Europe.
- ESBLAT (2018). ESBL-Attributieanalyse (ESBLAT). Projectno TKI-AF 12067.
- EMA (2018). Sales of veterinary antimicrobial agents in 30European countries in 2016.
- EU (2019) Verordening 2019/6 van het Europees parlement en de raad van 11 december 2018 betreffende diergeneesmiddelen. Publicatieblad van de Europese Unie L 4, 43-167.
- EZ (2016) Kamerbrief vervolgbeleid antibiotica in de veehouderij 8 juli 2016. Kenmerk: DGAN-DAD / 16098945
- EZ (2014) Kamerbrief over antibioticumgebruik in de veehouderij 9 december 2014. Kenmerk: DGA-DAD / 14193727
- Gezondheidsraad (2018). Gezondheidsrisico's rond veehouderijen: vervolgadvies.
- Gezondheidsraad (2015). Briefadvies Aanscherping antibioticagebruik bij dieren.
- Huijbers, P.M.C. et al. (2015). Role of the environment in the transmission of antimicrobial resistance to humans: a review. Environmental Science&Technology 49: 11993-12004.
- Kivits, T., Broers, H. P., Beeltje, H., Griffioen, J., & van Vliet, M. (2017). Antibiotica in grondwater onder intensieve veehouderijgebieden. Water Matters-kennismagazine voor waterprofessionals, 8-11.
- Knapp, C.W, Dolfing, J., Ehlert, P.A.I. en D.W. Graham (2010) Evidence of Increasing Antibiotic Resistance Gene Abundances in Archived Soils since 1940. Environmental Science and Technology, 44, 580-587
- Lahr J, Moermond C, Montforts M, Derksen A, Bondt N, Puister-Jansen L, de Koeijer T en Hoeksma P (2019) Diergeneesmiddelen in het milieu - Een synthese van de huidige kennis. STOWA rapportno. Xxx.
- Leenstra, F., R. Bergevoet, T. Kimman & P. Vriesekoop (2010), Diergezondheid in de veehouderij, op weg naar duurzaamheid, Lelystad: Wageningen UR Livestock Research. (essay op verzoek van het PBL)
- LNV (2019) Kamerbrief SDa-rapport antibioticagebruik bij landbouwhuisdieren 2018. 27 juni 2019. Kenmerk: DGA-DAD / 19142150
- LNV (2018) Kamerbrief-over-antibioticagebruik-bij-landbouwhuisdieren-in-2017. 26 juni 2018. Kenmerk: DGAN-DAD / 18123473
- MARAN-2018 (2018), Monitoring of Antimicrobial Resistance and Antibiotic Usage in Animals in the Netherlands in 2017
- MARAN-2017 (2017), Monitoring of Antimicrobial Resistance and Antibiotic Usage in Animals in the Netherlands in 2016
- MARAN-2015 (2015), Monitoring of Antimicrobial Resistance and Antibiotic Usage in Animals in the Netherlands in 2014
- MARAN_2019_Monitoring_of_antimicrobial_resistance_and_antibiotic_usage
- in_animals_in_the_Netherlands_in_2018
- NETHMAP-2019 (2019), Consumption of Antimicrobial Agents and Antimicrobial Resistance among Medically Important Bacteria in the Netherlands_
- Mevius, D. (2008), Resistentie, een gevoelig onderwerp. (inaugurele rede Universiteit Utrecht, geraadpleegd april 2010.
- Mughini-Gras, L., Dorado-Garcia, A., van Duijkeren, E., van den Bunt, G., Dierikx, C. M., Bonten, M. J., ... & de Koeijer, A. (2019). Attributable sources of community-acquired carriage of Escherichia coli containing β-lactam antibiotic resistance genes: a population-based modelling study. The Lancet Planetary Health, 3(8), e357-e369.
- PBL (2010) Op weg naar een duurzame veehouderij. Ontwikkelingen tussen 2000 en 2010.
- Schmitt, H., Blaak, H., Kemper, M., van Passel, M. W., Hierink, F., van Leuken, J., ... & de Man, H. (2017). Bronnen van antibioticaresistentie in het milieu en mogelijke maatregelen.
- SDa (2019) Het gebruik van antibiotica bij landbouwhuisdieren in 2018. SDa, Autoriteit Diergeneesmiddelen
- https://www.autoriteitdiergeneesmiddelen.nl/nl/publicaties/sda-rapporte…
- SDa (2018) Het gebruik van antibiotica bij landbouwhuisdieren in 2017. SDa, Autoriteit Diergeneesmiddelen
- SDa (2017) Het gebruik van antibiotica bij landbouwhuisdieren in 2016. SDa, Autoriteit Diergeneesmiddelen.
- SDa (2015) Het gebruik van antibiotica bij landbouwhuisdieren in 2014. SDa, Autoriteit Diergeneesmiddelen.
- Singer, A. C., Shaw, H., Rhodes, V., & Hart, A. (2016). Review of antimicrobial resistance in the environment and its relevance to environmental regulators. Frontiers in microbiology, 7. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5088501/
Relevante informatie
- EU. Europese wetgeving diergeneesmiddelen
- FIDIN. Antibioticagebruik in de veehouderij. FIDIN, branchevereniging van Veterinaire Farmacie in Nederland.
- RIVM. Informatie over antibioticaresistentie. Rijksinstituut voor Volksgezondheid en Milieu.
Technische toelichting
- Naam van het gegeven
- Antibioticagebruik in de veehouderij en resistentie van bacteriën tegen antibiotica
- Omschrijving
- Frequent gebruik van antibiotica leidt tot resistentie van bacteriën tegen deze middelen.
- Verantwoordelijk instituut
- Planbureau voor de Leefomgeving, Martha van Eerdt (PBL/WLV)
- Berekeningswijze
- Cijfers over het antibioticagebruik per kg levend gewicht en over antibioticaresistentie zijn afkomstig van FIDIN en MARAN-2019. De hoeveelheid antimicrobiële groeibevorderaars is geschat uit grafieken in de FIDIN-rapportages.
- Basistabel
- -
- Geografische verdeling
- Nederland
- Verschijningsfrequentie
- jaarlijks
- Achtergrondliteratuur
- FIDIN, branchevereniging van Veterinaire Farmacie in Nederland.MARAN-2019 (2019), Monitoring of Antimicrobial Resistance and Antibiotic Usage in Animals in the Netherlands in 2018
- Opmerking
- De verkoopdata van FIDIN omvatten naar schatting 98% van de verkopen in Nederland. De berekening van de hoeveelheid antibiotica is in overeenstemming gebracht met de door het Europees Medicijn Agentschap geharmoniseerde methode (EMA, 2018). Het gemiddeld gebruik per kg levend gewicht per land wordt sterk bepaald door de samenstelling van de veestapel en het type gebruikte antibiotica. Zo heeft een land met veel melkvee een lager gemiddelde dan een land met relatief veel varkens en kippen.Voor de volksgezondheid kritische middelen zijn 3e en 4e generatie cefalosporines, fluorochinolonen, beta-lactam antibiotica, aminoglycosiden en colistines.
- Betrouwbaarheidscodering
- Het aantal behandeldagen per dier in de periode 2009-2010 is gebaseerd op cijfers uit een LEI-steekproef, ca 400 bedrijven w.v. circa 80% intensieve veehouderijbedrijven (Bondt, 2012). Vanaf 2011 (melkkoeien 2012) zijn de rapportages van SDa (ca 40.000 bedrijven) de bron. De SDa heeft in 2015 het aantal behandeldagen (DDDA_NAT) uit haar rapportages herberekend zodat een vergelijking met de LEI reeks mogelijk is (SDa, 2015 p.38).
Archief van deze indicator
Bekijk meer Bekijk minder
Referentie van deze webpagina
CLO (2019). Gebruik van antibiotica in de veehouderij en resistentie, 1999 - 2018 (indicator 0565, versie 07, ), www.clo.nl. Centraal Bureau voor de Statistiek (CBS), Den Haag; PBL Planbureau voor de Leefomgeving, Den Haag; RIVM Rijksinstituut voor Volksgezondheid en Milieu, Bilthoven; en Wageningen University and Research, Wageningen.